নবম ও দশম শ্রেণীর সৃজনশীল প্রশ্নোত্তর (১৩ ই আগস্ট)
প্রিয় শিক্ষার্থীরা, Srijonshil.com এর প্রকাশিত সৃজনশীল লেসনে তোমাদের স্বাগতম। আজ আমরা রসায়নের একটি সৃজনশীল প্রশ্নোত্তর আলোচনা করব এবং তোমাদের অনুশীলনের জন্য পদার্থবিজ্ঞানের একটি প্রশ্ন প্রকাশ করব।
আজকের সৃজনশীল প্রশ্ন ও নমুনা উত্তর (রসায়ন)
নিচের উদ্দীপকটি পড়ো এবং প্রশ্নগুলোর উত্তর দাওঃ
নিচে পারমাণবিক সংখ্যা উল্লেখপূর্বক তিনটি মৌলের কাল্পনিক প্রতীক দেয়া হলোঃ
X (7), Y (8), Z (3)
ক. কোন নিষ্ক্রিয় গ্যাসের শেষ কক্ষপথের ইলেকট্রন সেট অষ্টক নয়?
খ. আয়নিক যৌগের গলনাংক ও স্ফুটনাংক সমযোজী যৌগ অপেক্ষা বেশি হওয়ার কারণ কী?
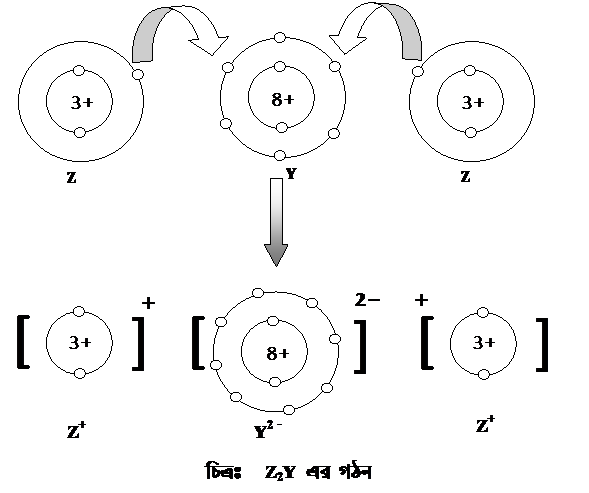
গ. Y ও Z এর মধ্যকার রাসায়নিক বন্ধন তৈরির প্রক্রিয়া বর্ণনা করো।
ঘ. “একাধিক মৌলের পারমাণবিক সংখ্যা থেকে তাদের মধ্যে গঠিত যৌগের ধর্ম সম্বন্ধে ধারণা পাওয়া যায়” – উক্তিটি উদ্দীপকে উল্লেখিত X ও Y মৌলের আলোকে বিশ্লেষণ করো।
নমুনা উত্তর
ক. হিলিয়ামের শেষ কক্ষপথের ইলেকট্রন সেট অষ্টক নয়।
খ. সমযোজী যৌগের অণুসমূহ পরস্পরের সাথে দুর্বল ভ্যানডার ওয়ালস বল দ্বারা আকৃষ্ট থাকে। পক্ষান্তরে, আয়নিক যৌগে প্রতিটি আয়ন তার চতুর্দিকে বিপরীত আধানযুক্ত আয়ন দ্বারা পরিবেষ্টিত হয়ে এক বিশেষ ধরনের জালিকা তৈরি করে শক্তিশালী বলে আবদ্ধ থাকে।
কোনো সমযোজী যৌগকে কঠিন থেকে তরলে ও তরল থেকে বায়বীয় অবস্থায় রূপান্তরিত করতে শুধুমাত্র দুর্বল ভ্যানডার ওয়ালস বলকে অতিক্রম করতে হয়। পক্ষান্তরে, কঠিন আয়নিক যৌগকে তরলে ও তরল থেকে বায়বীয় অবস্থায় নিতে প্রতিটি আয়নকে তার চতুর্দিকের বিপরীত আধানগুলোর সাথে বিদ্যমান শক্তিশালী বন্ধন ছিন্ন করতে হয় এবং সেক্ষেত্রে প্রচুর তাপশক্তি ব্যয় করতে হয়। এই কারণে আয়নিক যৌগের গলনাংক ও স্ফুটনাংক সমযোজী যৌগ অপেক্ষা বেশি।
গ. প্রতিটি পরমাণু নিকটবর্তী নিষ্ক্রিয় মৌলের ইলেকট্রন বিন্যাস লাভ করে স্থিতিশীল হতে চায়। এটি করার জন্য পরমাণুসমূহ ইলেকট্রনের আদান প্রদান কিংবা শেয়ার করে এবং রাসায়নিক বন্ধনে জড়িয়ে পড়ে।
প্রদত্ত উদ্দীপকের Y ও Z মৌল এবং তাদের নিকটবর্তী নিষ্ক্রিয় মৌলের ইলেকট্রন বিন্যাস নিম্নরূপঃ
Z (3) = 2, 1 He (2) = 2
Y (8) = 2, 6 Ne (10) = 2, 8

এখানে, Z মৌলটি He (হিলিয়াম) এর মত ইলেকট্রন বিন্যাস পেতে একটি ইলেকট্রন ত্যাগ করবে এবং Y মৌলটি Ne (নিয়ন) এর মত ইলেকট্রন বিন্যাস পেতে দুইটি Z পরমাণু থেকে একটি করে মোট দুইটি ইলেকট্রন গ্রহণ করবে। এতে Z পরমাণুটি ধনাত্মক ও Y পরমাণুটি ঋণাত্মক চার্জে চার্জিত হয়ে পরস্পরকে আকর্ষণ করবে ও একটি আয়নিক যৌগ তৈরি করবে যার আণবিক সংকেত হবে Z2Y।
ঘ. আমরা জানি, নিউট্রাল অবস্থায় একটি পরমাণুর ইলেকট্রন সংখ্যা তার পারমাণবিক সংখ্যার সমান। এই ইলেকট্রন সংখ্যা থেকে সহজে একটি পরমাণুর ইলেকট্রন বিন্যাস লেখা যায়। উদ্দীপকে উল্লেখিত X ও Y মৌলের পারমাণবিক সংখ্যা যথাক্রমে 7 ও 8। সুতরাং নিউট্রাল অবস্থায় এদের ইলেকট্রন সংখ্যা হবে যথাক্রমে 7 ও 8 এবং ইলেকট্রন বিন্যাস হবে নিম্নরূপঃ
X (7) = 2, 5
Y (8) = 2, 6
আবার আমরা জানি,যে সকল পরমাণুর সর্ববহিঃস্থ কক্ষপথে 5, 6 বা 7 টি ইলেকট্রন থাকে তারা অধাতু হয়। এবং একাধিক অধাতু পরমাণু পরস্পরের মধ্যে ইলেকট্রন শেয়ারের মাধ্যমে সমযোজী বন্ধনে আবদ্ধ হয়।
উপরোক্ত কারণে X ও Y মৌল দুটি অধাতু হবে এবং নিজেদের মধ্যে সমযোজী যৌগ গঠন করবে। এক্ষেত্রে সমযোজী যৌগের সাধারণ ধর্ম অনুসারে বলা যায়, X ও Y এর মধ্যকার গঠিত যৌগটির গলনাংক ও স্ফুটনাংক কম হবে, ইহা পানিতে দ্রবীভূত হবে না এবং বিদ্যুৎ অপরিবাহী হবে ইত্যাদি।
সুতরাং আমরা বলতে পারি, দু’টি পরমাণুর পারমাণবিক সংখ্যা থেকে এদের মধ্যকার গঠিত যৌগের প্রকৃতি ও ধর্ম সম্বন্ধে ধারণা পাওয়া যায়।
আজকের সৃজনশীল প্রশ্ন (পদার্থ বিজ্ঞান)
নিচের উদ্দীপকটি পড়ো এবং প্রশ্নগুলোর উত্তর দাওঃ
এক ভ্যান ড্রাইভার মাল বোঝাই করে 10 kmh-1 বেগে একটি রেল ক্রসিং পার হতে যাচ্ছিল। খালি ভ্যান ও মালপত্রের ওজন ছিল যথাক্রমে 100 kg ও 400 kg। ড্রাইভার যখন রেলক্রসিং থেকে 10 m দূরে ছিল তখন সে একটি ট্রেনকে ঐ ক্রসিং পার হতে দেখে সাথে সাথে ব্রেক চাপল। এতে ভ্যানটি 5 s এর মধ্যে পুরোপুরি থেমে গিয়ে সংঘর্ষ এড়াতে পারল। কিন্তু এটি করতে গিয়ে ভ্যান ড্রাইভারের নাভিশ্বাস অবস্থার সৃষ্টি হলো।
ক.বেগ কী?
খ.একটি ভ্যানের মন্দন 30 ms-2 উত্তরদিকে বলতে কী বুঝ?
গ. ব্রেক চাপার পর ভ্যানটি কত দূরত্ব গিয়ে থামবে?
ঘ. “ভ্যানটি যদি খালি থাকত তবে ভ্যান ড্রাইভার আরও সহজে ভ্যানটি থামাতে পারত” – উক্তিটি বিশ্লেষণ করো।
মতামত জানাতে এখানে ক্লিক করো।